

м. Київ, Симона Петлюри, 28

+380 (096) 515 79 79
+38 (093) 414 79 79
13 травня, 2020
Всi новини
За даними медичної статистики, заснованих на останніх результатах епідеміологічних досліджень, інтактний пародонтит зустрічався лише в 2-10% спостережень, захворювання пародонту та спостерігається у 90-95% дорослого населення. Збільшення поширеності генералізованих захворювань тканин пародонту доводиться переважно на вік від 30 до 50 років, і до 45 років досягає 96%. Серед молоді у віці від 16 до 20 років поширеність захворювань тканин пародонту різко збільшується і зустрічається в 50-85% випадків.
Підвищена поширеність генералізованих захворювань тканин пародонту, що характеризуються тривалим хронічним перебігом, зі схильністю до періодичного загострення з подальшим прогресуванням запально-дистрофічного процесу, який призводить до розвитку структурних і функціональних порушень зубощелепного апарату, є однією з основних медико-соціальних проблем. У зв’язку з цим розробка нових підходів до лікування генералізованого пародонтиту (далі за текстом – «ГП»), спрямованих на досягнення довгострокової стабілізації в перебігу ГП, займає одне з пріоритетних напрямків у розвитку сучасної стоматології.
Дослідження останніх років дозволили істотно поглибити уявлення про механізми виникнення та прогресування хронічних дистрофічно-запальних захворювань пародонту. Відповідно до сучасних уявлень етіологічні фактори ГП традиційно поділяються на місцеві та системні. До місцевих належать фактори, які діють безпосередньо на тканини пародонту, тоді як системні залежать від загального стану хворого. Серед найбільш значущих етіологічних факторів розвитку ГП дослідники виділяють вплив пародонтопатогенних мікроорганізмів і продуктів їх життєдіяльності на тканини пародонту, на стан порожнини рота, що сприяє утворенню зубної бляшки і впливає на пародонтопатогенний потенціал мікрофлори, загальні (системні) фактори, що забезпечують гомеостаз пародонту на тлі наявної генетичної схильності, зміни реактивності організму. Серед важливих факторів ризику розвитку ГП також називають порушення мікроциркуляції і транскапілярного обміну, дисбаланс імунокомпетентних систем, залучення автоімунітету, недостатність антиоксидантного захисту.
За «судинною» теорією патогенезу ГП – мікроциркуляторні розлади з’являються вже на ранніх стадіях ГП і супроводжують все періоди захворювання. Вони характеризуються гальмуванням швидкості кровотоку, агрегацією і стазом формених елементів крові, пошкодженням ендотеліальних клітин, що сприяє тромбоутворення. Висока поширеність захворювань, що супроводжуються дисфункцією ендотелію (ЕД), перш за все атеросклерозу, сприяє розвитку дисбалансу між механізмами антиоксидантного захисту і швидкістю СРО. Перекисне окислення фосфоліпідів клітинних мембран сприяє їх деструкції, пошкодження клітин пародонту, що в свою чергу знижує стійкість тканин до ушкодження етіологічними факторами, в т. р. І мікробним впливом.
Накопичення недоокислених продуктів сприяє і розвитку змін у кістковій тканині альвеолярного відростку з активацією процесів резорбції кістки і деструкції колагенових волокон. Активація СРО супроводжується зміною рН клітин ендотелію судин, тканин пародонту з розвитком метаболічного ацидозу і змін властивостей клітинних мембран. Сучасні уявлення про роль оксидативного стресу в патогенезі хронічного пародонтиту дозволяють розглядати зміст переокислення ліпідів в слині і її антиокислювальний потенціал в якості предикторів ескалації запального ураження пародонту.
Таким чином розробка нових підходів до лікування генералізованого пародонтиту (далі за текстом – «ГП»), спрямованих на досягнення довгострокової стабілізації в перебігу ГП, займає одне з пріоритетних напрямків у розвитку сучасної стоматології.
Серед них – клетинна інженерія, що базується на використанні для активації процесів репаративної регенерації клетинних структур факторів росту, які продукуються багатьма клітинами, наприклад, тромбоцитами.
Ще в 1990-х рр. було доведено, що в тромбоцитах нашої крові є фактори росту – білки, які стимулюють розвиток стовбурових клітин і перетворення їх в клітини тієї тканини організму, яка пошкоджена.
Терапевтичний ефект тромбоцитарної аутоплазми (ТАП) пояснюється присутністю тромбоцитів і вмістом в них факторів росту (ФР), але ефект плазми крові може бути заснований і на інших якісних складових, наприклад мікро- і макроелементи, вітаміни, що знаходяться в найбільш біодоступному для тканин стані.
На теперішній час основною метою досліджень процесів регенерації є необхідність ідентифікації ФР, знання механізму їх дії і можливостей застосування для поліпшення регенерації поверхні рани.
Використання ТАП сьогодні представляє одну з небагатьох можливостей запускати і прискорювати природні механізми регенерації за рахунок ФР, що містяться у тромбоцитах. Крім того, вона не токсична і не іммунореактивна. Отримання ТАП технологічно є поділом плазми і тромбоцитів від еритроцитів як по градієнту щільності, так і з використанням спеціалізованих лабораторних фільтрів.
ТАП модулює і регулює функцію первинних, вторинних і третинних ФР, впливаючи на всі стадії регенерації одночасно. Згадана властивість відрізняє ФР тромбоцитарної аутоплазми від рекомбінантних ЧЗ, що відповідають за окремий механізм регенерації.
Тромбоцити в своєму складі мають різноманітні ФР і цитокіни, які сприяють відновленню пошкоджених тканин. В α-гранулах тромбоцитів знаходяться понад 30 ФР, які впливають на процеси регенерації тканин пародонту одночасно. Найбільше значення мають: IGF (інсуліноподібний ФР) – який сприяє диференціюванню стовбурових клітин, збільшує метаболізм кісткової тканини і продукування колагену. PDGF (тромбоцитарний ЧЗ) – стимулює проліферацію і переміщення мезенхімальних (остеогенних) клітин, стимулює ангіогенез. PDEGF (тромбоцитарний ФР ендотеліальних клітин) – викликає стимулюючу дію на ендотеліальні клітини і має ангіогений ефект. VEGF або PDAF (ФР ендотелію судин) – є 4 види фактору: VEGF-A, -B, -C і -D. Беруть участь в ангіогенезі, індукують проліферацію ендотеліальних клітин судин. EGF (епідермальний ФР) – сприяє проліферації фібро- і остеобластів, збільшує синтез фібронектину. TGF-ß («Сімейство» трансформуючого ФР) – багатофункціональні чинники, оскільки не тільки індукують диференціювання мезенхімальних клітин, а також викликають велику кількість клітинних і міжклітинних відповідей, включаючи продукцію інших ФР. До трансформуючих ФР відносяться кісткові морфогенетичні білки, частина яких (КМБ-2, остеогенні або КМБ-3, КМБ-4,-5,-7,-8 і-9) є вираженими остеоіндукторами, модулюють клітинну проліферацію і диференціювання малодиференційованих клітин в остеобласти . PLGF-1 / -2 (плацентарні ФР) – потенціюють дію VEGF, підвищують проникність судинної стінки. FGF (фібробластний ФР) – викликає експресію в кістковій тканині, ангіогенез, остеофікацію, індукує продукцію TGF в остеобластних клітинах. Остеонектін – «культуральний шоковий протеїн»: складає 15% органічного компоненту кісткового матриксу, регулює проліферацію і взаємодію клітин з матриксом. Тромбоспондин – опосередковує адгезію кісткових клітин. ФР доставляються в тканини при ін’єкційній формі аутоплазми і концентруються за допомогою введення більшої кількості аутоплазми – це підвищує активність фібробластів і стимулює їх утворення. Фібробласти продукують колагенові волокна, гіалуронову кислоту і еластин. Все це призводить до утворення нової сполучної тканини, зростання капілярів. ФР також блокують остеокласти і стимулюють проліферацію остеобластів, що стримує надалі це зниження кісткової тканини і сприяє її регенерації. В результаті відновлюються обмінні процеси, поліпшуються мікроциркуляція і метаболізм в клітинах тканин, нормалізується тканинне дихання, активізується місцевий імунітет.
Протипоказаннями до використання методу є: злоякісні новоутворення; системні захворювання крові, психічні захворювання, алергічна реакція на антикоагулянт (натрій-гепарин) в анамнезі.
Для лікування пацієнтів використовувалася аутоплазма отримана за наступними методиками:
1)Отримання збагаченої тромбоцитами плазми PRP (Platelets Reach Plasma, Lifting-Plasma), яка в подальшому НЕ загусне. Для використання PRP-плазми використовують антикоагулянт. Її використовують для PRP-терапії. Методика отримання PRP передбачає, що плазма НЕ згорнеться ні до введення в організм пацієнта, ні після. Механізм дії – все ті ж фактори росту.
При отриманні збагаченої тромбоцитами плазми доречно використовувати пробірки, що містять антикоагулянт ACD – A. Вибір антикоагулянту не випадковий. Саме цей антикоагулянт дозволяє забезпечити максимальну виживаність і активність тромбоцитів. У банках крові саме це антикоагулянт використовується для зберігання тромбоцитарної маси. При одноразовому центрифугуванні в пробірці ми бачимо поділ на еритроцитарно-лейкоцитарний шар (темний) і плазму. Іноді між ними є яскраво виражений білястий шар, він називається Buffy Coat – це фракція антікоагульованного зразка крові, яка містить більшість лейкоцитів і тромбоцитів після центрифугування в градієнті щільності крові.
2) PRF (Platelets Reach Fibrin) – багатий тромбоцитами фібрин, у пробірці антикоагулянт не використовується:
-а. A-PRF (advance, тобто «покращений», PRF-згустки) – отримання збагаченої тромбоцитами плазми, яка загусне до застосування (антикоагулянт не використовується). Це загусла частина плазми крові, що містить багато чинників зростання для остео і ангіогенезу. З них можна приготувати мембрани і пробки за допомогою спеціального боксу PRF-BOX. Суть PRF-BOX у віджимі фібрину з метою його звільнення від зайвої плазми. Мембранами вкривають кісткові матеріали, дефекти неба після забору ясенних трансплантатів, мембрану Шнайдера при її перфорації і просто синус-ліфтах, використовують для хірургії пародонту. Пробки – для заповнення постекстракційних лунок зубів і пародонтальних дефектів. Так само, згустки можна нарізати ножицями на дрібні шматочки і змішувати їх з кістковими замінниками.
-б. i-PRF (injectable – ін’єкційний) – отримання збагаченої тромбоцитами плазми, яка загусне після застосування. Таку плазму використовують для змішування з кістковим замінником, з метою його стабілізації і надання йому певної форми. Для ін’єкцій в пародонтальні тканини із метою поліпшення їх кровопостачання, зміни біотипів ясен. Іноді для склеювання країв слизової оболонки, наприклад, мембрани Шнайдера.
Активація тромбоцитів у відповідь на пошкодження тканин відбувається під час процесу вивільнення PRF декількох біологічно активних білків, в тому числі; альфа-гранули тромбоцитів, ФР, отриманий з тромбоцитів (PGDF), трансформуючі ФР-β (TGF-β), судинний ендотеліальний ФР (VEGF) і епідермальний ФР. Насправді цитокіни тромбоцитів і лейкоцитів грають важливу роль у рольовій грі цього біоматеріалу, але підтримують їх фібриновий матрикс дуже корисний для формування визначальних елементів, що відповідають за реальний терапевтичний потенціал PRF. Цитокіни негайно використовуються і руйнуються в рані, що загоюється. Гармонія між цитокінами і підтримка їх фібриновою матрицею має набагато більш унікальне значення, ніж будь-яке інше похідне від тромбоцитів.
3) PPP – Platelet Poor Plasma – плазма з концентрацією тромбоцитів «норма». У пробірках з зеленим стікером початково є розділовий гель. Це зручно, тому що гель після центрифугування піднімається і щільно фіксує еритроцитарно-лейкоцитарний згусток, перешкоджаючи змішуванню з плазмою, АЛЕ параметри центрифугування для пробірок, що містять гель не дозволяють застосувати низькі швидкості центрифугування і в зв’язку з цим кінцевий продукт – плазма, не може містити високі концентрації тромбоцитів, однак вміст білків, амінокислот, мінералів і всього іншого залишається незмінним, що дає нам можливість застосовувати цю форму практично скрізь, так як вона відновлює все порушені функції тканин.
Сьогодні існує широкий арсенал методів і засобів, розроблених для комплексного лікування генералізованого пародонтиту та хронічного катарального гінгівіту, при цьому досягти стійкої стабілізації патологічного процесу в тканинах пародонту складно. Питання визначення оптимального підходу до лікування даної категорії хворих є досить актуальним і вимагає проведення подальших досліджень. Лікування захворювань пародонту важливо не тільки для підтримки здоров’я порожнини рота, але, як показує аналіз літературних джерел, і для зниження патологічних змін в тканинах пародонту, що дасть можливість розробити новий комплексний патогенетично-обґрунтований підхід до лікування генералізованого пародонтиту та хронічного катарального гінгівіту, спрямований на стійку стабілізацію дистрофічно-запального процесу в тканинах пародонту, який одночасно буде сприяти зміцненню здоров’я пацієнтів в цілому.
У дослідженні брали участі 27 осіб, з них 13 чоловік і 14 жінок у віці від 25 до 65 років, з діагнозами: хронічний катаральний гінгівіт середнього ступеня тяжкості, хронічний генералізований пародонтиту початкової-I і II ступеня тяжкості. Всі пацієнти були розділені на 2 групи: контрольна – 12 осіб і основна – 15 пацієнтів. Лікування гінгівіту і пародонтиту включало в себе лікування карієсу і його ускладнень; навчання пацієнтів гігієні порожнини рота і її контроль; проведення професійної гігієни та закритого кюретажу. Загальна протизапальна терапія призначалася пацієнтам з діагнозом генералізований пародонтит і проводилася з використанням антибактеріальних препаратів. Традиційна терапія доповнювалася призначенням Біоген Продентіс, розсмоктувати 3-4 рази на день протягом 10 днів. В основній групі: при гінгівіті і початкової-I ступеня пародонтиту після професійної гігієни, при пародонтиті – після закритого кюретажу, – застосовувалося введення iPRF в область перехідної складки. Всього проводили 3 процедури з інтервалом 10 днів, наступні 2 процедури вводили – PPP. Оцінка результатів: після кожної процедури – контрольний огляд; наступний візит – через 6 місяців. Якщо необхідно через 6 місяців проводили підтримуючу терапію – курс професійної гігієни з 1 процедурою PPP (якщо необхідно).
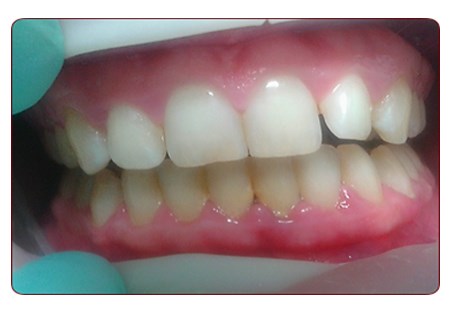
Фото 1. Пацієнтка М., 28 років. Діагноз: хронічний катаральний гінгівіт середнього ступеня тяжкості. До лікування.

Фото 2. Пацієнтка М., 28 років. Діагноз: хронічний катаральний гінгівіт середнього ступеня тяжкості. Відразу після лікування: зняття зубних відкладень і першої процедури плазмотерапії – iPRF.

Фото 3. Пацієнтка М., 28 років. Діагноз: хронічний катаральний гінгівіт середнього ступеня тяжкості.Через 3 роки після лікування.

Фото 4. Пацієнт 32 року. Генералізований пародонтит легкого ступеня тяжкості. Зубні відкладення. до лікування

Фото 5. Паціент 32 роки. Генералізований пародонтит легкого ступеня тяжкості. Зубні відкладення. Відразу після скейлінга і ін’єкцій I-PRF.

Фото 6. Пацієнт 32 року. Генералізований пародонтит легкого ступеня тяжкості. Зубні відкладення. Через 5 днів після лікування.
Вже через тиждень від початку лікування у пацієнтів основної групи, яким проводили ін’єкції тромбоцитарною аутоплазмою, відзначалася позитивна клінічна динаміка, яка виражалася в поліпшенні показників гігієнічного та пародонтальних індексів на 40%, в зниженні кровоточивості ясен на 60%, зменшення гіперемії ясен. У контрольній групі хворих в 70% випадків в цей термін зберігалися скарги на кровоточивість ясен, обмежену гіперемію папілярних ясен. Індексні показники не відрізнялися від вихідного рівня.
Через 6 місяців після проведеного лікування пацієнтів II (основний) групи ознаки запалення пародонту купувалося повністю: була відсутня кровоточивість, набряк, гіперемія ясен, зменшилася глибина зондування пародонтальних кишень. У контрольній групі хворих кровоточивість ясен знизилася на 50% в порівнянні з вихідними значеннями. Набряклість папілярного краю ясен і глибина пародонтальних кишень залишалися на вихідному рівні.
Через 12 місяців у пацієнтів основної групи клінічний стан пародонту було стабільним, що підтверджувалося відсутністю приросту показників пародонтальних індексів, відновленням функції зубів. У контрольній групі індексні значення, що характеризують стан пародонту, залишалися в 2,5 рази вищими, ніж в групі порівняння.
Результати дослідження показали ефективність і, відповідно, обґрунтованість застосування тромбоцитарної аутоплазми в комплексному лікуванні захворювань пародонту. Зниження індексних значень, що характеризують стан пародонту, в II групі пацієнтів відзначалося вже до 7 діб від початку лікування. Аналогічні показники в контрольній групі в цей термін практично не відрізнялися від вихідних. Через 12 місяців після лікування зниження (нормалізація) пародонтальних індексів у II групі відбулося на 82%, а в I (контрольної) – всього на 65%.
Висновок: Включення тромбоцитарної аутоплазми в комплексне лікування пародонтиту дозволяє лікувати запалення і стабілізувати процес в більш короткі терміни в порівнянні з загальноприйнятими методами лікування.